Frühe Nutzenbewertung - Cemiplimab beim Zervixkarzinom
Die frühe Nutzenbewertung von Cemiplimab (Libtayo®) ist das zweite Verfahren der frühen Nutzenbewertung für ein neues Arzneimittel zur systemischen Therapie des Zervixkarzinoms und ein weiteres Verfahren zu Cemiplimab. Cemiplimab ist indiziert als Monotherapie für die Behandlung von Patientinnen mit rezidiviertem oder metastasiertem Zervixkarzinom und Krankheitsprogression während oder nach einer platinbasierten Chemotherapie. Der G-BA hat das IQWiG mit dem Bericht beauftragt. Subgruppen, zweckmäßige Vergleichstherapie sowie Bewertungsvorschläge sind in Tabelle 1 zusammengefasst.
Tabelle 1: Vorschläge zum Zusatznutzen von Cemiplimab
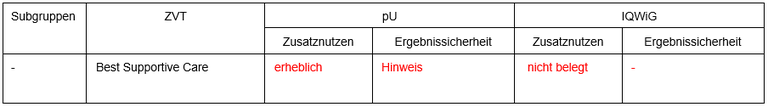
Legende: pU – pharmazeutischer Unternehmer, ZVT – zweckmäßige Vergleichstherapie
Unsere Anmerkungen sind:
- Die zweckmäßige Therapie „Best Supportive Care“ entspricht den Empfehlungen der Fachgesellschaften. Allerdings sind unterschiedliche Zytostatika auch in Deutschland Bestandteil der supportiven Therapie in diesem Krankheitsstadium und Inhalt der Leitlinien. Ziele sind Krankheitskontrolle und Symptomlinderung bei den meist jungen Patientinnen.
- Basis der frühen Nutzenbewertung ist EMPOWER-Cervical 1, eine randomisierte, offene Phase-III-Studie zum Vergleich der Wirksamkeit von Cemiplimab versus Chemotherapie nach ärztlicher Maßgabe und Best Supportive Care. Die Gesamtstudie bezog alle Patientinnen mit ein. Das Dossier ist begrenzt auf Patientinnen, die Pemetrexed, Topotecan, Irinotecan oder Vinorelbin erhielten. Das mittlere Alter der Patientinnen lag bei 50 Jahren.
- Cemiplimab führte zu einer signifikanten Verlängerung der Gesamtüberlebenszeit und zur Verbesserung von Parametern der Lebensqualität.
- Der Unterschied in der Gesamtüberlebenszeit zugunsten von Cemiplimab ist signifikant bei Patientinnen mit einer PD-L1-Expression >1%.
- Cemiplimab führte in der Gesamtstudie auch zur Steigerung der Ansprechrate, zur Verlängerung der progressionsfreien Überlebenszeit - und im Vergleich mit Chemotherapie - zur Reduktion schwerer Nebenwirkungen.
- Das Nebenwirkungsprofil von Cemiplimab entspricht den bisherigen Erfahrungen. Die Abbruchrate aufgrund unerwünschter Ereignisse lag in der Gesamtstudie im Cemiplimab-Arm bei 8,7% vs 5,2% im Kontrollarm.
- In der Bewertung des klinischen Nutzens auf der ESMO-Magnitude of Clinical Benefit Scale v1.1 erhält Cemiplimab auf der Basis von EMPOWER-Cervical 1 den Grad 5 (Skala 1 (niedrig) – 5 (hoch)).
Bei Patientinnen mit rezidiviertem oder metastasiertem Zervixkarzinom und Krankheitsprogression während oder nach einer platinbasierten Chemotherapie ist Cemiplimab der neue Standard.



