Frühe Nutzenbewertung - Alpelisib beim HR+/HER2- fortgeschrittenen Mammakarzinom
Alpelisib ist zugelassen zur Therapie von postmenopausalen Patientinnen und von männlichen Patienten mit Hormonrezeptor (HR)-positivem, HER2-negativem, lokal fortgeschrittenem oder metastasiertem Mammakarzinoms mit Nachweis einer PIK3CA-Mutation und nach Versagen der antihormonellen Therapie. Das IQWiG wurde mit dem Bericht beauftragt. Subgruppen, zweckmäßige Vergleichstherapie sowie die unterschiedlichen Bewertungsvorschläge sind in Tabelle 1 zusammengefasst.
Tabelle 1: Berechnung des Zusatznutzens durch pU und IQWiG
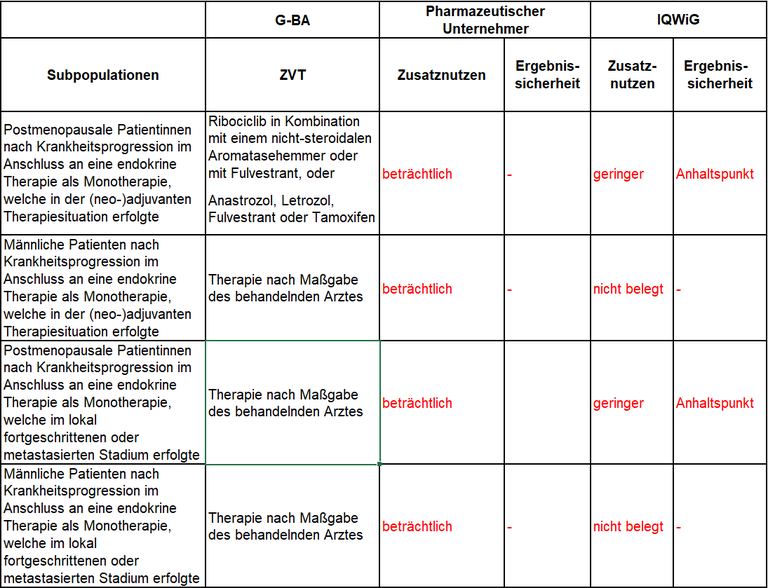
Unsere Anmerkungen sind:
- Die Bildung von Subgruppen auf der Basis des Krankheitsprogresses nach endokriner Therapie in der (neo-)adjuvanten (A) und der metastasierten Situation (B) ist biologisch und therapeutisch nur schlecht begründbar. Von größerer Relevanz sind die Zeit bis zum Eintritt der Refraktärität und Mechanismen der endokrinen Resistenz.
- In die Festlegung der zweckmäßigen Vergleichstherapie sind die neueren Daten noch nicht eingeflossen. Korrekt wäre hier „CDK4/6-Inhibitoren“ anstelle einer ausschließlichen Begrenzung auf Ribociclib. Das hat allerdings keinen Einfluss auf diese Nutzenbewertung, da im Kontrollarm keine CDK4/6-Inhibitoren eingesetzt wurden.
- Basis der frühen Nutzenbewertung zum Vergleich von Fulvestrant + Alpelisib vs Fulvestrant ist die randomisierte, Placebo-kontrollierte Phase-III-Studie SOLAR-1.
- Die Kombination von Fulvestrant + Alpelisib führte gegenüber Fulvestrant zur Steigerung der Remissionsrate und zur Verlängerung der progressionsfreien Überlebenszeit, nicht zur Verlängerung der Gesamtüberlebenszeit.
- Die Lebensqualität war in den beiden Studienarmen nicht signifikant unterschiedlich.
- Die Rate schwerer, Therapie-assoziierter Nebenwirkungen war im Alpelisib-Arm viel höher als im Kontroll-Arm, an erster Stelle steht eine Hyperglykämie. Therapieunterbrechungen und Dosisreduktionen sind häufig.
- In der Bewertung des klinischen Nutzens auf der ESMO-Magnitude of Clinical Benefit Scale v1.1 erhält Alpelisib in Kombination mit Fulvestrant den Grad 3 (Skala 1 (niedrig) – 5 (hoch)).
Alpelisib ist das erste Arzneimittel aus der neuen Substanzklasse der PIK3CA-Inhibitoren. Es erweitert das Spektrum der gezielten Arzneimittel bei Patientinnen und Patienten mit metastasiertem HR+/HER2- Mammakarzinom im Progress unter Aromatasehemmern. Das Nebenwirkungsspektrum macht eine engmaschige Überwachung der Patientinnen und Patienten erforderlich. Der rasche Wirkungseintritt erlaubt eine kurzfristige Beurteilung des Therapieansprechens.



