Frühe Nutzenbewertung - 177Lu-PSMA-617 beim metastasierten, kastrationsresistenten Prostatakarzinom (mCRPC)
Das Verfahren der frühen Nutzenbewertung von 177Lu-PSMA-617 ist das erste Verfahren zu diesem neuen Arzneimittel und ein weiteres Verfahren beim metastasierten, kastrationsresistenten Prostatakarzinom (mCRPC). 177Lu-PSMA-617 ist zugelassen zur Behandlung von Patienten mit metastasiertem kastrationsresistentem Prostatakarzinom, die zuvor mittels Inhibition des AR-Signalwegs und taxanbasierter Chemotherapie behandelt wurden. Die Therapie mit 177Lu-PSMA-617 wird in Kombination mit Androgendeprivationstherapie (ADT) mit oder ohne Inhibition des Androgenrezeptor-(AR)-Signalwegs durchgeführt. Der G-BA hat keine Subpopulationen gebildet. Das IQWiG wurde mit dem Bericht beauftragt. Pharmazeutischer Unternehmer und IQWiG kommen zu unterschiedlichen Vorschlägen. Einen Überblick über Vergleichstherapie und Bewertungsvorschläge gibt Tabelle 1.
Tabelle 1: Berechnung des Zusatznutzens durch pU und IQWiG
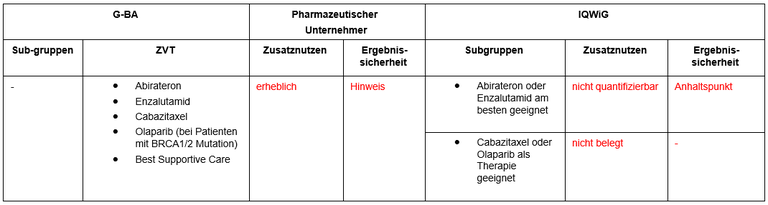
Unsere Anmerkungen sind:
- Die vom G-BA festgelegte ZVT entspricht den aktuellen Leitlinien.
- Basis der frühen Nutzenbewertung ist VISION, eine internationale, multizentrische, randomisierte, offene Phase-III-Studie mit 831 Patienten zum Vergleich von 177Lu-PSMA-617 gegenüber Standard of Care. Ebenfalls stehen Daten aus TheraP, einer in Australien durchgeführten, offenen, randomisierten Phase-II-Studie zum Vergleich von 177Lu-PSMA-617 gegenüber Cabazitaxel zur Verfügung.
- Voraussetzung für den Einsatz von 177Lu-PSMA-617 ist die qualitätsgesicherte PSMA-PET.
- In VISION führte 177Lu-PSMA-617 gegenüber der Standardtherapie zur signifikanten Erhöhung der radiologischen Ansprechrate, zur Verlängerung des radiologischen progressionsfreien Überlebens, zur Verlängerung der Gesamtüberlebenszeit und zur Verbesserung von Parametern der Lebensqualität.
- In TheraP führte 177Lu-PSMA-617 gegenüber Cabazitaxel zur signifikanten Erhöhung der radiologischen Ansprechrate, zur Verlängerung des radiologischen progressionsfreien Überlebens, zur Reduktion von Schmerzen und zur Verbesserung von Parametern der Lebensqualität. Die Gesamtüberlebenszeit wurde im Vergleich zu Cabazitaxel nicht verlängert.
- In VISION und TheraP haben Patienten mit einer hohen Standard Uptake Value (SUV) im PSMA-PET CT ein besseres Ansprechen. Dabei versteht man unter SUV ein semiquantitatives Maß für die Tracer-Aufnahme in einer Region von Interesse (Region of Interest, ROI).
- Die Nebenwirkungsrate unter 177Lu-PSMA-617 lag höher als unter Standard of Care, niedriger als unter Cabazitaxel. Die Abbruchrate aufgrund von Nebenwirkungen lag in VISION bei 11,9%.
- In der Bewertung des klinischen Nutzens auf der ESMO-Magnitude of Clinical Benefit Scale v1.1 erhält 177Lu-PSMA-617 den Grad 4 (Skala 1 (niedrig) – 5 (hoch)).
177Lu-PSMA-617 ist ein weiteres, hochwirksames Arzneimittel beim mCRPC nach Vortherapie mit neuen hormonellen Substanzen (NHA) und Taxanen.



